
वीडियो: रसायन विज्ञान में एक बहुपरमाणुक आयन क्या है?

2024 लेखक: Miles Stephen | [email protected]. अंतिम बार संशोधित: 2023-12-15 23:36
ए बहुपरमाणुक आयन , जिसे आणविक के रूप में भी जाना जाता है आयन , एक चार्ज है रासायनिक प्रजातियां ( आयन ) दो या दो से अधिक परमाणुओं से सहसंयोजक बंधित या एक धातु परिसर से बना होता है जिसे एक इकाई के रूप में कार्य करने वाला माना जा सकता है। उपसर्ग पॉली- का अर्थ ग्रीक में "कई," है, लेकिन यहां तक कि आयनों दोपरमाणुओं को आमतौर पर कहा जाता है बहुपरमाणुक.
बस इतना ही, एक बहुपरमाणुक आयन उदाहरण क्या है?
परमाणुक आयनों हैं आयनों जिसमें एक से अधिक परमाणु होते हैं। के लिये उदाहरण नाइट्रेट आयन , नहीं3-इसमें एक नाइट्रोजन परमाणु और तीन ऑक्सीजन परमाणु होते हैं। ए. में परमाणु बहुपरमाणुक आयन आमतौर पर सहसंयोजक रूप से एक दूसरे से बंधे होते हैं, और इसलिए एकल, आवेशित इकाई के रूप में एक साथ रहते हैं।
यह भी जानिए, बहुपरमाणुक आयनों के नामकरण के क्या नियम हैं? नियम 1. नाम में पहले धनायन लिखा जाता है, नाम में दूसरा ऋणायन लिखा जाता है। नियम 2. जब सूत्र इकाई में दो या अधिक समान हों बहुपरमाणुक , वह आयन कोष्ठक के बाहर लिखी गई सबस्क्रिप्ट के साथ कोष्ठक में लिखा गया है।
यह भी जानने के लिए कि यौगिक और बहुपरमाणुक आयन में क्या अंतर है?
यौगिकों ऐसी संस्थाएं हैं जिन्हें आम तौर पर अलग किया जा सकता है क्योंकि उन्हें किसी और चीज की आवश्यकता के बिना लिखा जाता है। उन्हें बनाया जा सकता है आयनों , अणु, आणविक आयनों , zwitterions, धातु परमाणु, आदि। आयनों आरोपित प्रजातियां हैं। विपरीत आवेश के काउंटरों के साथ मिलकर, वे बना सकते हैं यौगिकों.
क्या HCl एक बहुपरमाणुक आयन है?
एचसीएल , जिसमें आयन क्लोराइड होता है, कहलाता है हाइड्रोक्लोरिक एसिड . HNO3, जिसमें होता है बहुपरमाणुक नाइट्रेट को नाइट्रिक अम्ल कहते हैं।
सिफारिश की:
सामान्य रसायन विज्ञान और कार्बनिक रसायन विज्ञान में क्या अंतर है?
कार्बनिक रसायन विज्ञान को रसायन विज्ञान का एक उप-अनुशासन माना जाता है। जबकि सामान्य छत्र शब्द 'रसायन विज्ञान' सामान्य रूप से सभी पदार्थों की संरचना और परिवर्तनों से संबंधित है, कार्बनिक रसायन केवल कार्बनिक यौगिकों के अध्ययन तक ही सीमित है।
वह प्रक्रिया क्या है जिसके द्वारा नाइट्रेट आयन और नाइट्राइट आयन नाइट्रस ऑक्साइड गैस और नाइट्रोजन गैस n2 में परिवर्तित हो जाते हैं?

नाइट्रेट आयन और नाइट्राइट आयन नाइट्रस ऑक्साइड गैस और नाइट्रोजन गैस (N2) में परिवर्तित हो जाते हैं। डीएनए, अमीनो एसिड और प्रोटीन जैसे अणु बनाने में उपयोग के लिए पौधों की जड़ें अमोनियम आयनों और नाइट्रेट आयनों को अवशोषित करती हैं। कार्बनिक नाइट्रोजन (डीएनए में नाइट्रोजन, अमीनो एसिड, प्रोटीन) अमोनिया में टूट जाता है, फिर अमोनियम
आप एक बहुपरमाणुक आयन वाले यौगिक का सूत्र कैसे लिखते हैं?
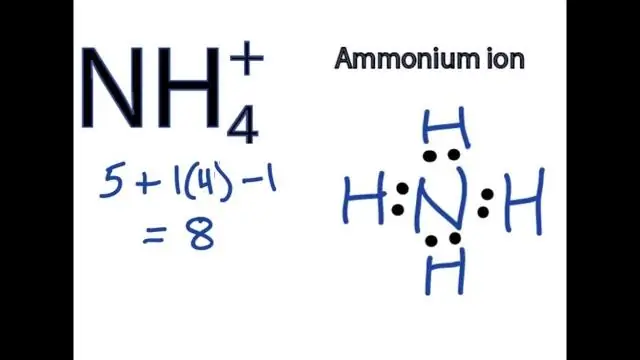
बहुपरमाणुक आयनों वाले यौगिकों के सूत्र लिखने के लिए, धातु आयन के लिए प्रतीक और उसके बाद बहुपरमाणुक आयन का सूत्र लिखें और आवेशों को संतुलित करें। एक बहुपरमाणुक आयन वाले यौगिक का नाम रखने के लिए पहले धनायन और फिर ऋणायन बताइए
सामान्य बहुपरमाणुक आयन क्या हैं?

सामान्य बहुपरमाणुक आयन Zn2+ जिंक। सीडी 2+ कैडमियम। 1+ चार्ज। एनएच4. अमोनियम। एचजी2. बुध (I) Ag+ सिल्वर। 1- चार्ज। C2H3O2। एसीटेट। सीएन- साइनाइड। क्लो- हाइपोक्लोराइट। क्लो 2. क्लोराइट। क्लो 3. क्लोरेट। क्लो 4। परक्लोरेट। एचसीओ3. हाइड्रोजन (द्वि) कार्बोनेट। एच2पीओ4
एक बहुपरमाणुक आयन में ऑक्सीकरण संख्या का योग कितना होता है?

एक बहुपरमाणुक आयन में ऑक्सीकरण संख्याओं का योग आयन पर आवेश के बराबर होता है। उदाहरण के लिए, SO42- आयन में सल्फर परमाणु की ऑक्सीकरण संख्या +6 होनी चाहिए, क्योंकि इस आयन में परमाणुओं की ऑक्सीकरण संख्या का योग -2 के बराबर होना चाहिए।
