
वीडियो: पोटेशियम में 4 गोले क्यों होते हैं?
2024 लेखक: Miles Stephen | [email protected]. अंतिम बार संशोधित: 2023-12-15 23:36
4s सबलेवल (जो केवल है एक कक्षीय) है 3d सबलेवल (5 ऑर्बिटल्स से मिलकर) की तुलना में कम ऊर्जा, इसलिए इलेक्ट्रॉन इस निचली ऊर्जा 4s ऑर्बिटल को पहले 'भर' देते हैं। और चूंकि 4s सबलेवल चौथे ऊर्जा स्तर का हिस्सा है (n= 4 ) आप K के विन्यास को 2, 8, 8, 1 के रूप में लिखते हैं।
तदनुसार, पोटेशियम के कितने गोले हैं?
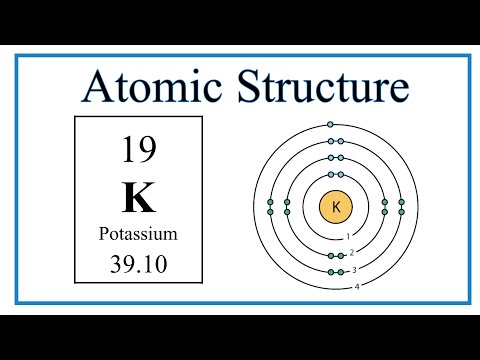
पोटैशियम आवर्त सारणी के पहले स्तंभ में चौथा तत्व है। इसे क्षार धातु के रूप में वर्गीकृत किया गया है। पोटैशियम परमाणुओं पास होना 19 इलेक्ट्रॉन और 19 प्रोटॉन बाहरी में एक वैलेंस इलेक्ट्रॉन के साथ सीप.
इसके अलावा, चौथे शेल में कितने इलेक्ट्रॉन हैं? चौथे ऊर्जा स्तर में 18 इलेक्ट्रॉन होते हैं। आवर्त सारणी के चौथे ऊर्जा स्तर में 4s 3d और 4p कक्षक शामिल हैं। 4p कक्षीय धारण करता है 6 इलेक्ट्रॉन . के साथ एक 4d कक्षीय है 10 इलेक्ट्रॉन जो आवर्त सारणी के 5वें ऊर्जा स्तर के साथ मेल खाता है।
इसी तरह, यह पूछा जाता है कि तीसरा शेल 8 या 18 क्यों है?
प्रत्येक सीप केवल एक निश्चित संख्या में इलेक्ट्रॉन हो सकते हैं: पहला सीप दो इलेक्ट्रॉनों को धारण कर सकता है, दूसरा सीप तक धारण कर सकते हैं आठ (2 + 6) इलेक्ट्रॉन, तीसरा खोल तक धारण कर सकते हैं 18 (2 + 6 + 10) और इसी तरह। इनमें इलेक्ट्रॉन क्यों मौजूद हैं, इसकी व्याख्या के लिए गोले इलेक्ट्रॉन विन्यास देखें।
पोटैशियम का अंतिम इलेक्ट्रॉन 3d स्तर के बजाय 4s में क्यों प्रवेश करता है?
उत्तर और स्पष्टीकरण: The अंतिम इलेक्ट्रॉन में पोटैशियम प्रविष्ट होता है 4एस कक्षा का इसके बजाय NS 3डी कक्षीय क्योंकि 4एस कक्षीय में कम ऊर्जा होती है की तुलना में स्तर NS 3डी कक्षीय औफबौ सिद्धांत कहता है कि इलेक्ट्रॉनों सबसे कम उपलब्ध ऊर्जा पर कब्जा करें स्तर जमीनी अवस्था में।
सिफारिश की:
एक गोले के कितने आयाम होते हैं?

एक गोला एक तीन आयामी ठोस आकृति है, क्योंकि इसके तीन आयाम हैं और यह 3-डी अंतरिक्ष में स्थित है। एक गोले में इसकी सतह के सभी बिंदु एक निश्चित बिंदु (इसका केंद्र) से समान दूरी पर होते हैं
कुछ तत्वों में ऐसे प्रतीक क्यों होते हैं जो तत्वों के नाम में अक्षरों का उपयोग नहीं करते हैं?

अन्य नाम-प्रतीक बेमेल वैज्ञानिकों द्वारा अरबी, ग्रीक और लैटिन में लिखे गए शास्त्रीय ग्रंथों के शोध पर और बाद के दो भाषाओं के मिश्रण का उपयोग करके "सज्जन वैज्ञानिकों" की आदत से "एक आम भाषा के रूप में" के बारे में आया। पत्रों के पुरुष।” पारा के लिए एचजी प्रतीक, उदाहरण के लिए
कौन से ज्वार वास्तव में उच्च होते हैं और महीने में दो बार आते हैं जब चंद्रमा और सूर्य संरेखित होते हैं?

बल्कि, यह शब्द ज्वार 'वसंत आगे' की अवधारणा से लिया गया है। मौसम की परवाह किए बिना वसंत ज्वार पूरे साल में हर चंद्र महीने में दो बार आते हैं। नीप ज्वार, जो महीने में दो बार भी आता है, तब होता है जब सूर्य और चंद्रमा एक दूसरे के समकोण पर होते हैं
सोडियम पोटेशियम पंप को सक्रिय परिवहन क्यों माना जाता है, सोडियम और पोटेशियम को किस दिशा में पंप किया जा रहा है?

सोडियम-पोटेशियम पंप। सक्रिय परिवहन ऊर्जा की आवश्यकता वाली प्रक्रिया है जिसमें अणुओं और आयनों को झिल्ली 'चढ़ाई' में पंप किया जाता है - एक एकाग्रता ढाल के खिलाफ। इन अणुओं को उनकी सांद्रता प्रवणता के विरुद्ध ले जाने के लिए, एक वाहक प्रोटीन की आवश्यकता होती है
साइटोप्लाज्म में कौन से अंगक होते हैं जिनमें एंजाइम होते हैं जो प्रोटीन को पचाते हैं?

लाइसोसोम मैक्रोमोलेक्यूल्स को उनके घटक भागों में तोड़ देते हैं, जिन्हें बाद में पुनर्नवीनीकरण किया जाता है। इन झिल्ली-बद्ध जीवों में विभिन्न प्रकार के एंजाइम होते हैं जिन्हें हाइड्रोलेस कहा जाता है जो प्रोटीन, न्यूक्लिक एसिड, लिपिड और जटिल शर्करा को पचा सकते हैं। लाइसोसोम का लुमेन साइटोप्लाज्म की तुलना में अधिक अम्लीय होता है
