विषयसूची:

वीडियो: कूलम्बिक आकर्षण आयनन ऊर्जा को कैसे प्रभावित करता है?

2024 लेखक: Miles Stephen | [email protected]. अंतिम बार संशोधित: 2023-12-15 23:36
जितना बड़ा आयनीकरण ऊर्जा , एक इलेक्ट्रॉन को निकालना उतना ही कठिन होता है। उसी का उपयोग करना कूलम्बिक आकर्षण विचार, हम पहले की व्याख्या कर सकते हैं आयनीकरण ऊर्जा आवर्त सारणी पर रुझान। परमाणु की वैद्युतीयऋणात्मकता जितनी अधिक होती है, उसकी इलेक्ट्रॉनों को अपनी ओर आकर्षित करने की क्षमता उतनी ही अधिक होती है।
इसके बाद, कोई यह भी पूछ सकता है कि कूलम्बिक आकर्षण इलेक्ट्रोनगेटिविटी को कैसे प्रभावित करता है?
कूलम्ब के नियम के अनुसार, जैसे-जैसे परमाणुओं की एक श्रृंखला के भीतर परमाणु क्रमांक बढ़ता है, परमाणु आकर्षण इलेक्ट्रॉनों के लिए भी वृद्धि होगी, इस प्रकार इलेक्ट्रॉन (ओं) को नाभिक के करीब खींचेंगे। NS कूलम्बिक आकर्षण अपने इलेक्ट्रॉनों के लिए एक परमाणु के नाभिक के रूप में जाना जाता है वैद्युतीयऋणात्मकता परमाणु का।
इसके बाद, प्रश्न यह है कि स्क्रीनिंग प्रभाव आयनीकरण ऊर्जा को कैसे प्रभावित करता है? अधिक इलेक्ट्रॉन परिरक्षण नाभिक से बाहरी इलेक्ट्रॉन खोल, कम ऊर्जा उक्त परमाणु से एक इलेक्ट्रॉन को बाहर निकालने के लिए आवश्यक है। उच्च परिरक्षण प्रभाव कम आयनीकरण ऊर्जा.
लोग यह भी पूछते हैं कि कौन से कारक कूलम्बिक आकर्षण को प्रभावित करते हैं?
कूलम्बिक आकर्षण को प्रभावित करने वाले कारक
- प्रोटॉन (जो सकारात्मक रूप से चार्ज होते हैं) और इलेक्ट्रॉन (जो नकारात्मक रूप से चार्ज होते हैं) प्रत्येक को आकर्षित करते हैं।
- धनावेशित आयन और ऋणावेशित आयन प्रत्येक की ओर आकर्षित होते हैं।
आवर्त में कूलम्बिक आकर्षण क्यों बढ़ता है?
- आप जैसे जाते हैं एक अवधि के दौरान , इलेक्ट्रॉन हैं उसी ऊर्जा स्तर में जोड़ा गया। नाभिक में अधिक प्रोटॉन की सांद्रता "उच्च प्रभावी परमाणु आवेश" बनाती है। दूसरे शब्दों में, वहाँ है का एक मजबूत बल आकर्षण इलेक्ट्रॉनों को नाभिक के करीब खींचना जिसके परिणामस्वरूप एक छोटा परमाणु त्रिज्या होता है।
सिफारिश की:
रासायनिक प्रतिक्रिया के दौरान ऊर्जा का अवशोषण और रिलीज तापमान परिवर्तन को कैसे प्रभावित करता है?

ऊष्माशोषी अभिक्रियाओं में उत्पादों की एन्थैल्पी अभिकारकों की एन्थैल्पी से अधिक होती है। क्योंकि प्रतिक्रियाएं ऊर्जा को छोड़ती या अवशोषित करती हैं, वे अपने परिवेश के तापमान को प्रभावित करती हैं। एक्ज़ोथिर्मिक प्रतिक्रियाएं उनके परिवेश को गर्म करती हैं जबकि एंडोथर्मिक प्रतिक्रियाएं उन्हें ठंडा करती हैं
कूलम्बिक आकर्षण को कौन से कारक प्रभावित करते हैं?

जैसे-जैसे समय-समय पर ऊर्जा का स्तर जोड़ा जाता है, नाभिक और वैलेंस इलेक्ट्रॉनों के बीच की दूरी बढ़ती है, कूलम्बिक आकर्षण कम हो जाता है गैर-धातु इलेक्ट्रॉन प्राप्त करते हैं और नकारात्मक आयन बनाते हैं। ऋणात्मक आयनों को आयन कहते हैं
तापमान गैस के अणुओं की गतिज ऊर्जा को कैसे प्रभावित करता है?

काइनेटिक आणविक सिद्धांत के अनुसार, तापमान में वृद्धि से अणुओं की औसत गतिज ऊर्जा में वृद्धि होगी। जैसे-जैसे कण तेजी से आगे बढ़ते हैं, वे संभवतः कंटेनर के किनारे से अधिक बार टकराएंगे। कणों की गतिज ऊर्जा बढ़ने से गैस का दबाव बढ़ जाएगा
कूलम्बिक आकर्षण परमाणु त्रिज्या से कैसे संबंधित है?

कूलम्ब के नियम के अनुसार, जैसे-जैसे परमाणुओं की एक श्रृंखला के भीतर परमाणु संख्या बढ़ती है, इलेक्ट्रॉनों के लिए परमाणु आकर्षण भी बढ़ेगा, इस प्रकार इलेक्ट्रॉन (ओं) को नाभिक के करीब खींचेंगे। परमाणु क्रमांक और परमाणु त्रिज्या के बीच ऐसा संबंध एक सीधा संबंध है
किस प्रकार का जीव सूर्य के प्रकाश से ऊर्जा का उपयोग करता है और इसे रासायनिक ऊर्जा में परिवर्तित करता है?
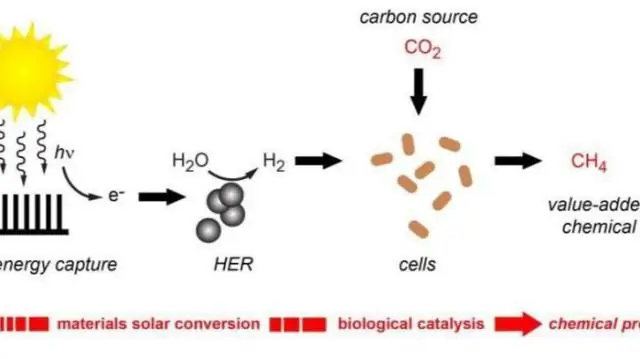
प्रकाश संश्लेषण वह प्रक्रिया है जिसके द्वारा जीव जिसमें वर्णक क्लोरोफिल होता है, प्रकाश ऊर्जा को रासायनिक ऊर्जा में परिवर्तित करता है जिसे कार्बनिक अणुओं (जैसे, शर्करा) के आणविक बंधनों में संग्रहीत किया जा सकता है।
