वीडियो: द्रव्यमान संख्या बढ़ने पर बाध्यकारी ऊर्जा का क्या होता है?
2024 लेखक: Miles Stephen | [email protected]. अंतिम बार संशोधित: 2023-12-15 23:36
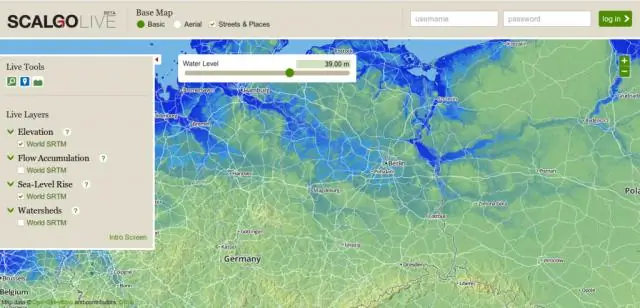
उपरोक्त आंकड़ा दर्शाता है कि जैसे परमाणु द्रव्यमान संख्या बढ़ जाती है , NS बाँधने वाली ऊर्जा प्रति न्यूक्लिऑन कम हो जाती है ए> 60 के लिए। दूसरे शब्दों में, बीई / ए में कमी आई है। बीई/ए के ए नाभिक इसकी स्थिरता की डिग्री का एक संकेत है। आम तौर पर, अधिक स्थिर न्यूक्लाइड में कम स्थिर वाले की तुलना में अधिक बीई / ए होता है।
इसके अलावा, बाध्यकारी ऊर्जा द्रव्यमान संख्या के साथ कैसे भिन्न होती है?
NS बाँधने वाली ऊर्जा प्रति नाभिक को विभाजित करके निर्धारित किया जाता है बाँधने वाली ऊर्जा नाभिक के द्वारा संख्या इसमें शामिल न्यूक्लियॉन के। मध्यवर्ती परमाणु वाले तत्व जनता सबसे बड़ा है बाध्यकारी ऊर्जा प्रति न्यूक्लियॉन और इसलिए सबसे स्थिर हैं।
कोई यह भी पूछ सकता है कि क्या बाध्यकारी ऊर्जा का द्रव्यमान होता है? द्रव्यमान दोष और बाँधने वाली ऊर्जा . नाभिकीय बाँधने वाली ऊर्जा है ऊर्जा परमाणु के नाभिक को प्रोटॉन और न्यूट्रॉन में विभाजित करने के लिए आवश्यक है। NS बाँधने वाली ऊर्जा एक प्रणाली के अतिरिक्त के रूप में प्रकट हो सकता है द्रव्यमान , जो इस अंतर के लिए जिम्मेदार है।
नतीजतन, द्रव्यमान संख्या बढ़ने पर प्रति न्यूक्लियॉन बाध्यकारी ऊर्जा का क्या होता है?
NS प्रति न्यूक्लियॉन बाध्यकारी ऊर्जा हल्के न्यूक्लाइड के लिए कम है और बढ़ोतरी उसके साथ जन अंक . इस प्रकार प्रति न्यूक्लियॉन बाध्यकारी ऊर्जा के साथ घटता है बढ़ोतरी में जन अंक अधिकतम तक पहुंचने के बाद।
बाध्यकारी ऊर्जा का क्या होता है?
बाँधने वाली ऊर्जा . नाभिकीय बाँधने वाली ऊर्जा है ऊर्जा एक परमाणु के एक नाभिक को उसके घटक भागों में विभाजित करने के लिए आवश्यक है: प्रोटॉन और न्यूट्रॉन, या सामूहिक रूप से, न्यूक्लियॉन। NS बाँधने वाली ऊर्जा नाभिकों की संख्या सदैव धनात्मक होती है, क्योंकि सभी नाभिकों को नेट की आवश्यकता होती है ऊर्जा उन्हें अलग-अलग प्रोटॉन और न्यूट्रॉन में अलग करने के लिए।
सिफारिश की:
एक प्रोटॉन के द्रव्यमान और एक इलेक्ट्रॉन के द्रव्यमान के बीच क्या अंतर है?
प्रोटॉन और न्यूट्रॉन का द्रव्यमान लगभग समान होता है, लेकिन वे दोनों इलेक्ट्रॉनों की तुलना में बहुत अधिक विशाल होते हैं (इलेक्ट्रॉन के रूप में लगभग 2,000 गुना बड़े पैमाने पर)। एक प्रोटॉन पर धनात्मक आवेश एक इलेक्ट्रॉन पर ऋणात्मक आवेश के परिमाण के बराबर होता है
पोटेशियम के एक परमाणु की द्रव्यमान संख्या क्या है जिसमें 20 न्यूट्रॉन हैं?

20 न्यूट्रॉन के साथ पोटेशियम के एक परमाणु की द्रव्यमान संख्या 39 होगी और इस प्रकार पोटेशियम-39 आइसोटोप का परमाणु होगा
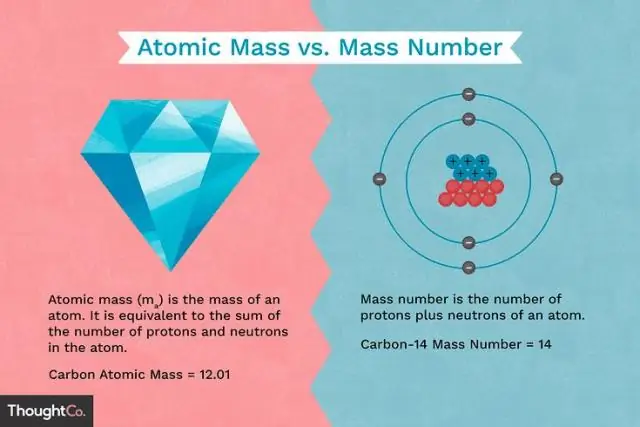
द्रव्यमान संख्या और परमाणु संख्या क्या है?

द्रव्यमान संख्या (अक्षर A द्वारा निरूपित) को एक परमाणु में प्रोटॉन और न्यूट्रॉन की कुल संख्या के रूप में परिभाषित किया जाता है। नीचे दी गई तालिका पर विचार करें, जो आवर्त सारणी के पहले छह तत्वों से डेटा दिखाती है। हीलियम तत्व पर विचार करें। इसका परमाणु क्रमांक 2 है, अतः इसके नाभिक में दो प्रोटॉन होते हैं
उच्चतम द्रव्यमान संख्या वाले सिलिकन के परमाणु में प्रोटॉनों की संख्या कितनी होती है?

उदाहरण के लिए, सिलिकॉन में 14 प्रोटॉन और 14 न्यूट्रॉन होते हैं। इसका परमाणु क्रमांक 14 है और इसका परमाणु द्रव्यमान 28 है। यूरेनियम के सबसे सामान्य समस्थानिक में 92 प्रोटॉन और 146 न्यूट्रॉन हैं। इसका परमाणु क्रमांक 92 है और इसका परमाणु द्रव्यमान 238 (92 + 146) है। 2.1 इलेक्ट्रॉन, प्रोटॉन, न्यूट्रॉन और परमाणु। तत्व लौह प्रतीक Fe प्रत्येक कोश में इलेक्ट्रॉनों की संख्या प्रथम 2 द्वितीय 8 तृतीय 14
एक उच्च द्रव्यमान वाला तारा निम्न द्रव्यमान वाले तारे से भिन्न रूप से क्यों विकसित होता है?

एक उच्च द्रव्यमान वाला तारा कम द्रव्यमान वाले तारे से अलग क्यों विकसित होता है? ए) यह अधिक ईंधन जला सकता है क्योंकि इसका मूल गर्म हो सकता है। इसका गुरुत्वाकर्षण कम है इसलिए यह अंतरिक्ष से अधिक ईंधन नहीं खींच सकता
